무세포 진피 기질을 활용한 재건 수술에 대한 문헌적 고찰
Use of Acellular Dermal Matrix in Reconstructive Surgery: A Review
Article information
Trans Abstract
In recent decades, tissue engineering advances have led to more skin substitutes becoming available. Acellular dermal matrix, initially developed for use in the treatment of full-thickness burns, is made by removing the cellular components from the dermis collected from donated bodies or animals. This class of scaffold is used to replace skin and soft tissue deficiencies in a variety of fields, including breast reconstruction, abdominal wall reconstruction, and burn treatment. Herein, we provide a detailed review of the clinical applications of acellular dermal matrix.
서론
여러 원인에 의해 피부가 손상된 상태를 창상이라 한다. 피부가 손상되면 빠른 시간 안에 원래의 피부 구조와 유사하게 치유되어야 하는데, 그렇지 않으면 감염 등의 이차적 합병증이 발생하거나 미적, 기능적인 면에서 문제가 생길 수 있다[1].
최근 수십 년간 조직 생물학, 제조 공학 및 재료 과학이 발전함에 따라 많은 수술에서 이용될 수 있는 피부 대체재가 점차 확대되고 있다[2]. 피부 대체재는 창상의 유형과 원인 또는 대체가 필요한 피부 등에 따라 알맞게 선택하며, 원하는 미적, 기능적 결과도 고려 해야 한다[3]. 특히 화상이나 암 절제 등으로 피부 결손이 넓게 발생한 경우에는 일반적으로 피부이식이나 피판술을 시행하며, 최근에는 여러 종류의 진피 이식을 활용하고 있다[1]. 그중 현재 유방 재건, 복벽 재건, 화상 등 다양한 분야에서 사용하고 있는 무세포 진피 기질(acellular dermal matrix)에 대해 살펴보고자 한다.
우선 무세포 진피 기질이 나오게 된 배경을 보면, 화상 치료와 가장 연관이 있다. 부위가 넓은 심부 화상 치료의 경우 메쉬부분 층피부이식술(mesh split-thickness skin graft)로 결손 부위를 덮어주었으나 후일 이식 부위에 반흔 흉터나 수축으로 인해 문제가 종종 발생하였다. 수축이 일어나는 가장 큰 요인은 진피 성분이 부족하여 발생한다. 그렇다면 피부이식 시 진피를 충분히 포함하여 피부이식을 시행한다면 피부공여부는 진피부족으로 인해 상처가 치유되지 않아 이에 또다른 심각한 문제가 발생하게 될 수 있어서 진퇴양난의 상황에 처할 수 있다. 진피를 포함한 사체의 피부 (allograft skin)를 이식한 경우 초기에는 생착이 되었으나 일시적이며 결국 면역반응으로 인해 이식은 실패를 하게 된다. 피부 장기의 주된 면역반응을 일으키는 부위는 표피(epidermis) 및 진피의 내피세포(endothelial cell)와 섬유아세포(fibroblast)이다. 따라서 피부이식 시 진피의 성분을 포함하여 수축을 줄이고, 면역반응으로 인해 피부생착이 실패하는 것을 방지하고자 피부이식 시 진피를 포함하여 크게 떼어낸 뒤 먼저 적절한 효소 처리를 하여 표피 부위를 제거하고, 진피 중에서 면역반응을 일으키는 세포를 제거하면, 무세포 진피 기질(acellular dermal matrix)이 남게 되며 이들의 주 성분으로는 콜라겐(collagen), 일레스틴(elastin), 프로테오글라이칸(proteoglycan)이며, 이런 과정을 거친 무세포 진피 기질을 피부연조직 결손 부위에 이식을 하며, 놀랍게도 살아있는 세포가 없어도 이식한 곳에서 살아남고, 게다가 주위 조직이 안으로 자라 들어오게 하는 바탕이 되게 하며, 그 뒤에 얇은 부분 층 피부이식술을 덧대어 결손 부위를 해결하는 것이다[4].
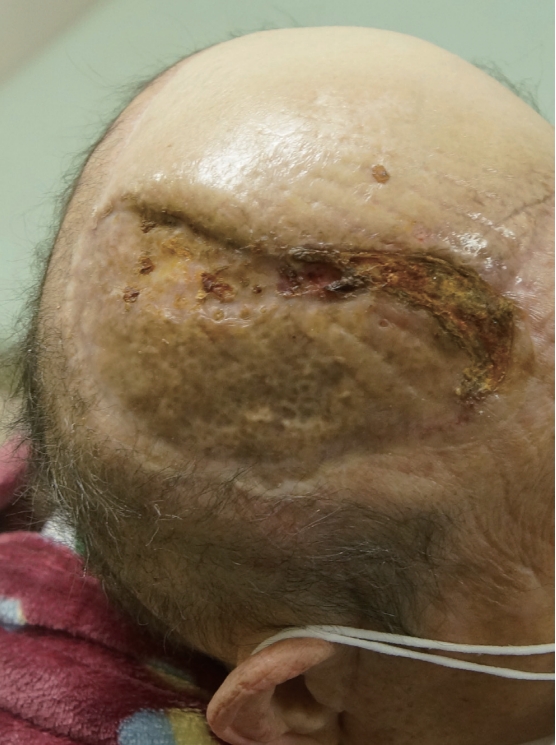
사체진피에서 무세포진피기질을 추출하는 방법은 처음에는 화학약품을 사용하는 방법을 사용하였으나, 방법상 감염 등의 문제가 발생할 수 있는 내재적 요소가 있었으나 최근 메가덤(L&C Bio, Seoul, Korea)이란 제품은 사체의 피부에 화학약품의 첨가물 대신 전자 빔을 조사하는 방법을 통해 감염의 확률을 줄이고 진피의 크로스 링킹(cross linking) 과정을 덜 파괴시키는 방법으로, 이로 인해 기존 화학약품을 통합 방법에 비해 진피의 크로스 링킹 3차원 구조를 어느 정도 보존시켜 인장강도(tensile strength)를 상승시킬 수 있다고 보고하였고, 안와 파열 골절에서도 사용되어 좋은 결과를 보고하고 있다[5]. 본 저자들도 두피 재건에 메가덤을 사용하여 좋은 결과를 얻은 경험이 있다(Figs. 1, 2)

Immediate appearance after application of acellular dermal matrix to a patient with a full-thickness scalp defect.
본론
1. 무세포 진피 기질에 대한 기본적 이해
진피는 콜라겐, 엘라스틴, 글리코사미노글리칸(glycosaminoglycan) 등의 세포외기질이 풍부한 층으로, 표피를 구조적으로 지지해 줌과 동시에 혈관을 통해 영양분을 공급한다. 또한 반 강성 (semirigid)이면서 탄력이 있어 충격으로부터 신체를 보호하고, 혈관의 수축 및 확장, 땀샘 증발을 통해 체온조절에서도 중요한 역할을 한다[2]. 인공 진피는 1980년 Yannas와 Burke가 글리코사미노글리칸을 첨가한 콜라겐을 재료로 하여 처음 만들었고, 그 후 Bell 등이 콜라겐과 표피를 배양해 인공 진피를 만들고 그 위에 다시 배양된 표피를 이식하는 시도를 하였다[6,7]. 그리고 무세포 진피 기질이 이후 3도 화상 치료에 사용하기 위해 처음 개발되었다.
진피 내에는 온도 감각, 고유 감각(proprioception)과 같은 특수한 기능을 위한 여러 신경 종말들이 있다. 진피가 창상 치유에 필요한 요소들로 구성되어 있지만, 땀샘이나 신경 종말 등의 세포들이 항원성이 높아 거부반응 없이는 동종 이식이나 이종 이식이 불가능하다[2]. 그래서 이러한 문제를 해결하기 위해 기증된 시신 혹은 동물에게서 진피를 채취한 후 화학적 방법 혹은 방사선 조사를 통해 면역반응을 일으키는 세포 성분을 제거하였고, 이것을 무세포 진피 기질이라 한다[4,5]. 세포 성분을 제거하고 난 이후에는 결정화(crystallization)를 방지하고 안정적인 보관을 위해 동결건조 처리된다[2]. 무세포 진피 기질은 다양한 이름을 가진 많은 상품들이 있지만 비슷한 방법으로 처리를 하고 있다. 인간 진피에서 유래된 제품으로는 알로덤(AlloDerm)Ⓡ, NeoForm, Flex HD, SureDerm, Glyaderm 등이 있고, 돼지 진피 제품으로 Collamend, Strattice, 소 진피 제품으로 Pelnac, Renoskin, Matriderm, Surgimend 등이 있다[2].
현재 무세포 진피 기질은 다양한 용도로 사용되고 있으며, 특히 조직이나 장기 재생 분야에서 광범위하게 연구되고 있다. 무세포성 기질은 정상 조직의 미세 환경을 모방하는 생리적 신호를 생성하기 때문에 수술 환경에서 일반적으로 사용하던 합성 생체재료 (synthetic biomaterial)에 비해 조직 재생과 기능적인 면에서 더욱 적합하다[7]. 또한 합성 재료는 항상 감염이나 돌출(extrusion)의 위험이 있는 반면, 무세포 진피 기질은 생체 적합성이 우수하며 정상 조직과 결합되어 그럴 위험이 적다[2].
2. 무세포 진피 기질의 임상적 이용
1) 유방 재건
최근 몇 년간 보형물을 이용한 재건술에서 무세포 진피 기질이 중요하게 사용되고 있으며, 유방 절제술 후 가슴 벽의 빈 공간에 삽입한 보형물에 대해 좀 더 쉽게 이중으로 커버하여 보호해 줄 수 있어서, 수술 결과를 향상해 줄 수 있기 때문이다. 또한 수술 집도의가 조직 확장기나 보형물을 흉벽 위에 최적으로 위치시키게 하여, 1단계 혹은 2단계 재건술을 용이하게 해주기 때문이다[8].
무세포 진피 기질은 유방 크기나 환자의 나이에 관계 없이 보형물을 이용한 유방 재건술을 받을 수 있는 대부분의 환자에서 사용이 가능하다. 일반적으로 즉시 유방 재건술에서 최대 이점이 발휘 되지만, 피부에 여유분이 있는 환자의 경우 지연 유방 재건술에서도 사용이 가능하다.
유방 절제술 후 보형물의 위치는 보통 대흉근 (pectora lis major muscle) 아래로 위치시키는데, 보형물이 완전히 근육 아래에 있어야 하는지, 부분적으로 아래에 위치해야 하는지는 아직 의견이 분분하다. 이 중 부분적으로 근육 아래에 보형물을 위치시키는 방법은 보형물의 돌출 정도를 개선시키고 유방밑주름 (inframammary fold)을 따라 보형물이 위치하며, 채워지는 부피를 어느 정도 증가시키는 장점이 있다. 하지만 유방 절제 피판의 하단 부분이 얇은 경우 유방 하부를 따라 겹쳐짐(rippling)이 생길 위험이 커지게 된다[8]. 이러한 단점을 보완하기 위해 무세포 진피 기질을 사용한다. 층이 추가되고 두께가 두꺼워져 이론적으로 잔주름을 최소화하며 유방의 위치를 자연스럽게 할 수 있다[8].
유방 하부의 피하 포켓(subcutaneous pocket)을 보강할 필요가 있을 때 무세포 진피 기질을 사용하게 되는 것인데, 과정은 다음과 같다. 무세포 진피 기질을 식염수에 적신 후 보형물의 크기에 따라 근육이 커버하지 못하는 부위에 맞춰 디자인을 한다. 기저막 (basement membrane) 부분이 보형물에 접하게 하고 위쪽으로는 대흉근 하단, 아래쪽으로는 유방밑주름에 해당하는 흉벽, 바깥쪽으로는 전거근(serratus anterior muscle)에 단단히 고정한다[9]. 이렇게 함으로써 보형물을 완전히 덮을 수 있게 된다. 무세포 진피 기질은 마치 힘줄의 역할을 하여, 대흉근을 유방밑주름에서 흉벽에 고정시키고 안정적인 구조를 형성한다. 이후 폐쇄형 배액관 (closed suction drain)이 무세포 진피 기질의 위아래로 위치하며, 배액량이 최소가 될 때까지 유지된다[10].
하지만 일부 환자들에게는 무세포 진피 기질이 효과적이지 않을수 있다. 고도비만 환자, 이전에 유방 절제술 및 방사선 치료를 받은 환자, 유방 절제술 후 피판으로의 혈류공급이 심히 안 좋은 환자, 현재 흡연 중인 환자 등이 이에 해당한다[8]. 이러한 환자들은 보형물을 이용한 재건술을 시행하였을 때 이득보다 위험이 더 크다. 체질량지수(body mass index)가 40을 넘는 비만 환자는 주위 피하층 두께가 보통 3 cm를 넘어가기 때문에 보형물이 유방 절제 공간 안으로 깊게 자리해서 충분히 돌출되지 못한다. 유방 절제 피판 두께 또한 1-2 cm를 넘어가고 진피하 혈관총(subdermal plexus) 까지의 거리가 멀어지게 되어 혈류공급이 원활히 되지 않는다. 그 결과, 무세포 진피 기질의 점착이 잘 이루어지지 않는다[8]. 유방 절제술 후 방사선 치료를 받은 환자의 경우에는 피부의 섬유화가 증가하고 탄력이 감소하며 혈관분포에 제한이 생긴다. 따라서 피부가 충분히 팽창하는 능력이 상대적으로 부족해져 지연 유방 재건술을 시행하기에는 다소 제한적인 면이 있다[8].
2. 복벽 재건
복벽 재건의 적응증으로는 종양 절제, 복벽 탈장 (ventral hernia) 및 절개 창 탈장(incisional hernia), 외상, 복강 내 감염으로 인한 패혈증, 괴사성 근막염(necrotizing fasciitis) 등이 있으며, 무세포 진피 기질은 보통 탈장 교정과 전복벽 결손(anterior abdominal wall defect)의 일차 복원에서 사용된다(Fig. 3) [11].
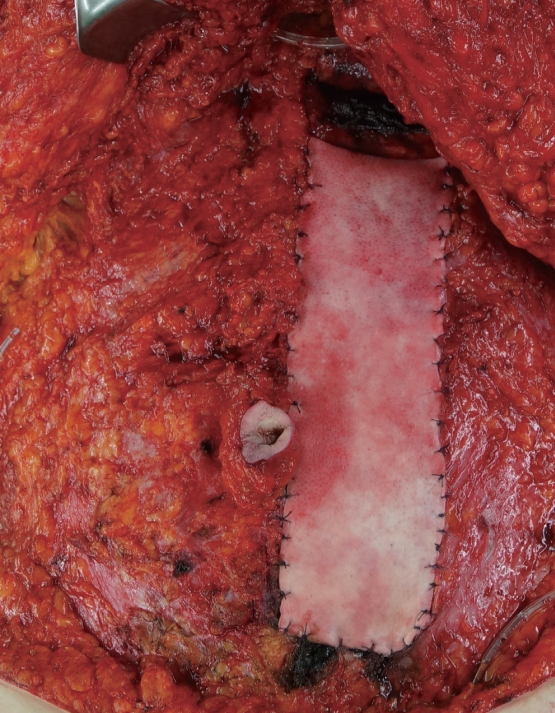
A case of abdominal wall reconstruction using acellular dermal matrix to prevent hernia of the abdominal wall after transverse rectus abdominis myocutaneous flap for breast reconstruction.
복벽 탈장의 결손부를 직접 봉합하여 복구하였을 때보다 합성 메쉬(mesh)를 이용해 강화해 주는 것이 훨씬 낮은 재발률을 보인다는 것이 여러 연구를 통해 입증되었다[11,12]. 하지만 합성 메쉬가 절대적으로 금기이거나(현재 감염 상태인 경우), 다음 선택으로 미뤄야 할 때(오염이 우려되거나 감염 위험성이 높은 경우)가 예상외로 많다. 이러한 환자들에게 메쉬를 대신하여 무세포 진피 기질을 사용하는 경우가 계속 증가해 왔다[13]. 무세포 진피 기질은 혈관 재생 및 주변 조직과의 결합 능력 덕분에 메쉬와 달리 감염에 저항성이 있고 돌출(extrusion) 및 침식(erosion)이 적으며, 시간이 지나면서 자연적인 콜라겐으로 재생되는 특징을 가진다[12,13].
무세포 동종 진피(human acellular dermal matrix)는 지금까지 머리와 목의 연조직 대체뿐만 아니라 화상에서도 성공적으로 사용되어 왔기 때문에 널리 알려져 있으며, 대표적인 상품으로 알로덤(AlloDermⓇ)이 있다. 알로덤 역시 진피기질의 구조와 뼈대를 손상하지 않고 그대로 유지하여 만들어지며, 세포와 혈관 재생이 쉽게 이루어지게 하는 장점을 가진다. 동물실험을 통해 복벽에서 특히 혈관을 빠르게 재생시키고 내장 유착(visceral adhesion)에 저항하는 알로덤의 능력이 확인되자, 2000년대 중반까지 메쉬 사용이 금기가 되는 많은 수술에서 알로덤이 사용되었다[14].
하지만 점점 사용이 늘어나면서 이 재료 본연의 탄력성(elasticity)이 문제가 되었는데, 이 성질은 유방 재건과 같은 특정 상황에서는 유리하게 작용하지만 복벽에 있어서만큼은 그렇지 않았다. 특히 큰 근막결손을 메울 때 복벽이 툭 튀어나오거나 느슨해질 수 있다는 위험성이 제기되었다. 이러한 문제를 해결하기 위해 등장한 것이 무세포 이종(돼지) 진피이다. 여기에 속하는 상품인 StratticeTM도 동일한 처리과정을 거쳐 만들어지는데, 다른 점은 콜라겐 기질 밀도가 높고 엘라스틴 함량이 낮아 알로덤보다 탄력성이 작다. 여전히 불룩해지지 않도록 사용에 주의를 기울여야 하지만 알로덤보다는 낫기 때문에 사용빈도가 늘어나고 있다[14].
무세포 진피 기질을 활용한 수술 기법은 상당히 다양하다. 완전한 근막 접합이 가능한 경우, 무세포 진피 기질은 보통 근막 아래 또는 위로 배치된다. 어떤 경우는 샌드위치 기법을 활용해 근막의 위아래로 놓이기도 한다. 완전한 근막 접합이 불가능한 경우, 결손을 교량처럼 연결시키는 삽입 방식으로 사용된다. 또한 components separation과 같은 기존에 정립되어 있는 다른 기법과 결부되어 사용되기도 한다[11].
3. 화상 및 만성 창상
무세포 진피 기질은 지난 20년간 개방형 연조직 결손에 사용되어 왔다. 많은 논문들이 3도 화상에서 진피 대체물로 알로덤을 사용하였다고 보고하였다. 이와 같은 무세포 동종 진피는 관절 부위를 포함하는 3도 화상에서 창상 피복에 효과적이고 관절 위 구축을 방지하는 충분한 탄력을 제공한다[2]. 또한 화상 외에 당뇨병성 족부 궤양의 치료에도 사용되고 있으며[2], 환부에 뼈와 인대가 드러나 있어 일반적인 피부이식이 어려운 환자를 대상으로 한다[4]. 무세포 동종 진피를 사용하였을 때의 장점은 면역학적으로 안전하면서 2차 수술의 필요성이 없다는 점이다. 또한 매우 얇은 부분 층 피부이식이 가능하여 공여부의 유병률이 감소하고, 공여부의 상처가 빨리 치유된다. 단점은 두꺼운 자가 부분 층 피부이식보다 혈관 신생이 늦다는 것이지만 혈관 신생이 되면 상피화는 정상적으로 일어 나게 된다[6].
결론
창상 치유를 돕는 피부 대체물로서 다양한 재료들이 사용되고 있다. 그 중 무세포 진피 기질(acellular dermal matrix)은 인간 혹은 동물의 진피 기질에서 항원성을 낮추기 위해 세포 성분을 제거하여 만들어지며, 생체적합성이 우수하고 혈관 재생을 용이하게 하는 장점을 가지고 있다. 하지만 가장 큰 단점 중에는 비용적 측면이 문제될 수 있다는 점이다. 이런 문제에도 불구하고 향후 가격적으로 좀 더 저렴한 방법이 나온다면 향후 무세포 진피 기질 세포를 통한 재건 방법이 현재보다 더 널리 사용될 수 있으리라 전망되며, 현재까지도 유방 재건, 복벽 재건, 화상 및 만성 창상 등의 다양한 분야에서 사용하고 있고, 앞으로도 다양한 상황에서 활용될 전망이다.